Reaksi kimia dapat digolongkan menjadi berbagai macam reaksi. Salah
satu diantaranya adalah reaksi yang berkaitan dengan perubahan bilangan
oksidasi dari atom-atom sebelum dan sesudah reaksi. Dari tinjauan
bilangan oksidasi reaksi dapat dibedakan menjadi 2 jenis reaksi yaitu :
- Golongan reaksi dimana atom-atom yang terlibat tidak mengalami
perubahan bilangan oksidasi sebelum dan sesudah reaksi. Reaksi dimana
atom-atom yang terlibat tidak mengalami perubahan bilangan oksidasi
disebut reaksi bukan reduksi-oksidasi yang lazim disebut reaksi bukan
redoks.
- Golongan reaksi dimana diantara atom-atom yang terlibat ada yang
mengalami perubahan bilangan oksidasi. Sebelum dan sesudah reaksi
bilangan oksidasi atom-atom yang terlibat tidak sama (berubah). Reaksi
ini disebut reaksi reduksi-oksidasi (reaksi redoks)
- A. PENGERTIAN REAKSI REDOKS
Redoks ( reduksi-oksidasi). Reduksi adalah penerimaan elektron atau
penurunan bilangan oksidasi, sedangkan oksidasi adalah pelepasan
elektron atau peningkatan bilangan oksidasi
CONTOH : REAKSI REDUKSI
Cu2+(aq) + 2e ® Cu (s) Ag+(aq) + e ® Ag(s)
CONTOH : REAKSI OKSIDASI
Zn(s) ® Zn2+(aq)+ 2e Al(s) ® Al3+(aq) + 3e
Aturan-aturan penentuan bilangan oksidasi :
- Atom-atom dalam unsur memiliki bilangan oksidasi nol
- Atom H dalam senyawa memiliki bilangan oksidasi +1
- Dalam hidrida logam (misal NaH, BaH2, AlH3) bilangan oksidasi H = -1
- Atom O dalam senyawa memiliki
- Dalam senyawa F2O, bilangan oksidasi O = +2
- Dalam peroksida (misal H2O2, Na2O2, BaO2) bilangan oksidasi O= -1
- Atom logam dalam senyawa memiliki bilangan oksidasi positif
- Jumlah bilangan oksidasi atom-atom dalam senyawa = Nol
- Jumlah bilangan oksidasi atom-atom dalam ion = muatan ion
- Jika dua atom berikatan, bilangan oksidasi negatif selalu dimiliki atom yang keelektronegatifannya lebih besar
Konsep-konsep dasar Redoks
- Oksidasi adalah peristiwa pelepasan elektron atau penambahan (kenaikan) bilangan oksidasi
- Reduksi adalah peristiwa penangkapan elektron atau pengurangan (penurunan) bilangan oksidasi
- Reduktor (pereduksi) adalah zat yang mengalami oksidasi atau zat
yang melepaskan elektron, atau zat yang bilangan oksidasinya naik
- Oksidator adalah zat yang mengalami reduksi atau zat yang menangkap elektron atau zat yang bilangan oksidasinya turun
- Redoks adalah reaksi yang terdiri dari peristiwa reduksi dan oksidasi atau reaksi perubahan bilangan oksidasi
- Reaksi disproporsionasi (autoredoks) adalah reaksi redoks dimana
hanya satu jenis atom yang mengalami reduksi dan oksidasi atau reaksi
redoks dimana hanya satu jenis atom yang bilangan oksidasinya berubah
- Mol elektron adalah selisih bilangan oksidasi
PENYETARAAN REAKSI REDOKS
1.METODE BILANGAN OKSIDASI
Langkah-langkah penyetaraan reaksi :
- Menentukan unsur yang mengalami oksidasi dan reduksi berdasarkan perubahan bilangan oksidasi tiap unsur
- Menyetarakan jumlah unsur yang mengalami redoks dengan menambahkan koefisien yang sesuai
- Menentukan besarnya kenaikan atau penurunan bilangan oksidasi dari unsur-unsur yang mengalami perubahan bilangan oksidasi
- Meneyetarakan perubahan bilangan oksidasi tersebut dengan memberikan koefisien yang sesuai
- Menyetarakan jumlah atom H dan O serta unsur-unsur yang lain
Contoh soal
 2 .METODE SETENGAH REAKSI (ION ELEKTRON)
2 .METODE SETENGAH REAKSI (ION ELEKTRON)
Langkah-langkah penyetaraan reaksi:
- Menuliskan zat-zat yang mengalami reaksi redoks saja
- Memisahkan reaksi menjadi 2, setengah reaksi reduksi dan setengah reaksi oksidasi
- Menyetarakan atom-atom yang mengalami redoks, kecuali atom hydrogen (H) dan oksigen (O)
- Menyetarakan atom oksigen (O) dengan menambahkan molekul H2O ke ruas yang kekurangan oksigen
- Menyetarakan atom Hidrogen (H) dengan menambahkan ion H+ ke ruas yang kekurangan atom H
- Menyetarakan muatan dengan menambahkan elektron ke ruas yang memiliki muatan lebih positif
- Menyamakan jumlah elektron pada kedua persamaan setengah reaksi reduksi dan oksidasi
- Menyatukan kedua persamaan setengah reaksi menjadi reaksi redoks yang utuh
- Mengembalikan ke bentuk reaksi awal
CONTOH SOAL

 PENGERTIAN SEL ELKTROKIMIA
PENGERTIAN SEL ELKTROKIMIA
Transfer elektron pada reaksi redoks dalam larutan berlangsung
melalui kontak langsung antara partikel-partikel berupa atom , molekul
atau ion yang saling serah terima elektron. Pembahasan transfer elektron
melalui sirkuit luar sebagai gejala listrik, dan reaksi redoks yang
seperti ini akan dipelajari pada elektrokimia.
Sel elektrokimia merupakan suatu sel atau tempat terjadinya aliran
elektron yang disebabkan oleh perubahan energi kimia menjadi energi
listrik atau sebaliknya. Sel ini dikelompokkan menjadi dua macam yaitu :
1. Sel Volta
2. Sel Elektrolisis
Sel Volta melibatkan perubahan energi kimia menjadi energi listrik
sedangkan sel elektrolisis melibatkan perubahan energi listrik menjadi
energi kimia. Bagaimanakah proses terjadinya perubahan energi tersebut?
SEL VOLTA
Sel Volta (sel galvani) memanfaatkan reaksi spontan (∆G < 0)
untuk membangkitkan energi listrik, selisih energi reaktan (tinggi)
dengan produk (rendah) diubah menjadi energi listrik. Sistem reaksi
melakukan kerja terhadap lingkungan
Sel Elektrolisa memanfaatkan energi listrik untuk menjalankan
reaksi non spontan (∆G > 0) lingkungan melakukan kerja terhadap
sistem
Kedua tipe sel menggunakan elektroda, yaitu zat yang menghantarkan
listrik antara sel dan lingkungan dan dicelupkan dalam elektrolit
(campuran ion) yang terlibat dalam reaksi atau yang membawa muatan.
KOMPONEN SEL VOLTA
Rangkaian sel elektrokimia pertama kali dipelajari oleh
LUIGI GALVANI (1780) dan
ALESSANDRO VOLTA (1800).
Sehingga disebut sel Galvani atau sel Volta. Keduanya menemukan adanya
pembentukan energi dari reaksi kimia tersebut. Energi yang dihasilkan
dari reaksi kimia sel Volta berupa energi listrik
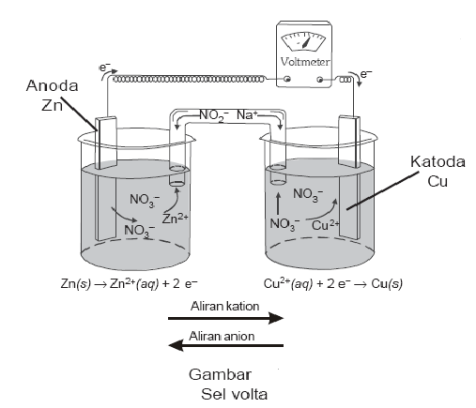
Sel Volta terdiri atas elektroda (logam seng dan tembaga) larutan
elektrolit (ZnSO4 dan CuSO4), dan jembatan garam (agar-agar yang
mengandung KCl). Logam seng dan tembaga bertindak sebagai elektroda.
Keduanya dihubungkan melalui sebuah voltmeter. Elektroda tempat
berlangsungnya oksidasi disebut Anoda (elektroda negatif), sedangkan
elektroda tempat berlangsungnya reduksi disebut Katoda (elektroda
positif)
ELEKTRODA
Elektroda terbagi menjadi dua jenis yaitu anoda dan katoda
Setengah reaksi oksidasi terjadi di anoda. Elektron diberikan oleh
senyawa teroksidasi (zat pereduksi) dan meninggalkan sel melalui anoda
Setengah reaksi reduksi terjadi di katoda. Elektron diambil oleh
senyawa tereduksi (zat pengoksidasi) dan masuk sel melalui katoda.
Setengah sel oksidasi: anoda berupa batang logam Zn dicelupkan dalam ZnSO4
Setengah sel reduksi: katoda berupa batang logam Cu dicelupkan dalam CuSO4
Terbentuk muatan relatif pada kedua elektroda dimana anoda bermuatan negatif dan katoda bermuatan positif
Kedua sel juga dihubungkan oleh jembatan garam yaitu tabung
berbentuk U terbalik berisi pasta elektrolit yang tidak bereaksi dengan
sel redoks gunanya untuk menyeimbangkan muatan ion (kation dan anion)
Dimungkinkan menggunakan elektroda inaktif yang tidak ikut bereaksi dalam sel volta ini misalnya grafit dan platinum.
NOTASI SEL VOLTA
•Sel Volta dinotasikan dengan cara yang telah disepakati (untuk sel Zn/Cu2+)
Zn(s)|Zn2+(aq)║Cu2+(aq)|Cu(s)
Bagian anoda (setengah sel oksidasi) dituliskan disebelah kiri bagian katoda
Garis lurus menunjukkan batas fasa yaitu adanya fasa yang berbeda (aqueous vs solid) jika fasanya sama maka digunakan tanda koma
Untuk elektroda yang tidak bereaksi ditulis dalam notasi diujung kiri dan ujung kanan.
POTENSIAL SEL
Sel volta menjadikan perubahan energi bebas reaksi spontan menjadi energi listrik
Energi listrik ini berbanding lurus dengan beda potensial antara
kedua elektroda (voltase) atau disebut juga potensial sel (Esel) atau
gaya electromotive (emf)
Untuk proses spontan Esel > 0, semakin positif Esel semakin banyak kerja yang bisa dilakukan oleh sel
Satuan yang dgunakan 1 V = 1 J/C
Potensial sel sangat dipengaruhi oleh suhu dan konsentrasi, oleh
karena itu potensial sel standar diukur pada keadaan standar (298 K, 1
atm untuk gas, 1 M untuk larutan dan padatan murni untuk solid).
POTENSIAL SEL STANDAR
Potensial elektroda standar adalah potensial yang terkait dengan setengah reaksi yang ada (wadah elektroda)
Menurut kesepakatan potensial elektroda standar selalu ditulis dalam setengah reaksi reduksi
Bentuk teroksidasi + ne à bentuk tereduksi E 1/2 sel
Potensial elektroda standar seperti halnya besaran termodinamika dapat dibalik dengan mengubah tandanya
E sel = E katoda – E anoda
Ilmuwan telah menyepakati untuk memilih setengah reaksi rujukan dengan nilai 0 untuk reaksi:
2H+(aq, 1 M) + 2e à H2(g, 1 atm) Eorujukan = 0
H2(g, 1 atm) à 2H+(aq, 1 M) + 2e –Eorujukan = 0
Dengan nilai rujukan ini kita bisa menyusun sel volta yang
menggunakan elektroda hidrogen standar sebagai salah satu elektrodanya
dan mengukur potensial sel dengan alat ukur, kemudian kita dapat
menentukan potensial elektroda standar banyak zat secara luas.
Semua nilai adalah relatif terhadap elektroda hidrogen standar (referensi)
2H+ (aq, 1 M) + 2e Û H2 (g, 1 atm)
Menurut konvensi semua setengah reaksi ditulis sebagai reaksi
reduksi artinya semua reaktan pengoksidasi dan semua produk pereduksi
Nilai Eo yang diberikan adalah setengah reaksi tertulis, semakin
positif nilainya semakin besar kecenderungan reaksi tersebut terjadi
Nilai Eo memiliki nilai yang sama tetapi berbeda tanda jika reaksinya kita balik
Berdasarkan tabel semakin keatas semakin oksidator dan semakin kebawah semakin reduktor.
REAKSI REDOKS SPONTAN
Setiap reaksi redoks adalah jumlah dari kedua setengah reaksi, sehingga akan ada reduktor dan oksidator ditiap-tiap sisi reaksi
Berdasarkan tabel maka reaksi spontan (Eosel> 0) akan terjadi
antara oksidator (sisi reaktan) dan reduktor (sisi produk) yang terletak
dibawahnya
Misal Cu2+ (kiri) dan Zn (kanan) bereaksi spontan dan Zn terletak dibawah Cu2+
Logam yang dapat menggantikan H2 dari asam. Ambil salah satu logam,
tuliskan reaksi oksidasinya lalu jumlah untuk memperoleh Eosel jika
positif maka H2 akan terlepas
Logam yang tidak dapat menggantikan H2, dengan langkah yang sama, namun jika hasilnya Eosel < 0, maka reaksi tidak spontan
Logam yang dapat menggantikan H2 dari air, logam yang terletak dibawah reduksi air
Logam yang dapat menggantikan logam lain dari larutannya, yaitu
logam yang terletak dibagian bawah tabel dapat mereduksi logam yang
terletak dibagian atas tabel.
Pengaruh Konsentrasi terhadap Potensial Sel
Sejauh ini potensial sel standar diukur dari potensial setengah sel
juga pada keadaan standar sementara kebanyakan sel volta tidak
beroperasi pada keadaan standarnya
Berdasarkan persamaan yang telah diketahui:
∆G = ∆Go + RT ln Q sedangkan
∆G = -nFEsel juga ∆Go = -nFEosel sehingga
-nFEsel = -nFEosel + RT ln Q
Esel = Eosel – (RT/nF) ln Q
Aplikasi Persamaan Nernst
Saat Q < 1 sehingga [reaktan] > [produk] maka Esel > Eosel
Saat Q = 1 sehingga [reaktan] = [produk] maka Esel = Eosel
Saat Q > 1 sehingga [reaktan] < [produk] maka Esel < Eosel
Jika kita memasukkan nilai R dan T pada 298
Esel = Eosel – (0,0592 V/n) log Q (pada 25oC)
SEL ELEKTROLISIS
Dalam tulisan ini, kita akan mempelajari tentang reaksi-reaksi sel
elektrolisis (aspek kualitatif). Kemudian kita akan menghitung massa
endapan logam dan volume gas yang dihasilkan dari reaksi elektrolisis
(aspek kuantitatif). Kita juga akan mempelajari pengaruh besarnya arus
listrik terhadap kuantitas produk elektrolisis yang dihasilkan.
 Sel Elektrolisis
Sel Elektrolisis adalah
sel yang menggunakan arus listrik untuk menghasilkan reaksi redoks yang
diinginkan dan digunakan secara luas di dalam masyarakat kita. Baterai
aki yang dapat diisi ulang merupakan salah satu contoh aplikasi sel
elektrolisis dalam kehidupan sehari-hari (
lihat Elektrokimia I : Penyetaraan Reaksi Redoks dan Sel Volta). Baterai aki yang sedang diisi kembali (
recharge) mengubah energi listrik yang diberikan menjadi produk berupa bahan kimia yang diinginkan. Air, H
2O,
dapat diuraikan dengan menggunakan listrik dalam sel elektrolisis.
Proses ini akan mengurai air menjadi unsur-unsur pembentuknya. Reaksi
yang terjadi adalah sebagai berikut : 2 H
2O
(l) ——> 2 H
2(g) + O
2(g)
Rangkaian
sel elektrolisis hampir menyerupai
sel volta. Yang membedakan
sel elektrolisisdari
sel volta adalah, pada
sel elektrolisis, komponen
voltmeter diganti dengan
sumber arus (umumnya baterai).
Larutan atau lelehan yang ingin dielektrolisis, ditempatkan dalam suatu
wadah. Selanjutnya, elektroda dicelupkan ke dalam larutan maupun
lelehan elektrolit yang ingin dielektrolisis. Elektroda yang digunakan
umumnya merupakan elektroda inert, seperti Grafit (C), Platina (Pt), dan
Emas (Au). Elektroda berperan sebagai tempat berlangsungnya reaksi.
Reaksi
reduksi berlangsung di
katoda, sedangkan reaksi
oksidasi berlangsung di
anoda.
Kutub
negatif sumber arus mengarah pada katoda (sebab memerlukan elektron)
dan kutub positif sumber arus tentunya mengarah pada anoda. Akibatnya,
katoda bermuatan negatif dan menarik
kation-kation yang akan
tereduksi menjadi endapan logam. Sebaliknya,
anoda bermuatan positif dan menarik
anion-anion yang akan
teroksidasi menjadi gas. Terlihat jelas bahwa tujuan elektrolisis adalah untuk mendapatkan endapan logam di katoda dan gas di anoda.

Ada dua tipe elektrolisis, yaitu
elektrolisis lelehan (leburan) dan
elektrolisis larutan. Pada proses
elektrolisis lelehan,
kation pasti tereduksi di katoda dan anion pasti teroksidasi di anoda. Sebagai contoh, berikut ini adalah reaksi elektrolisis lelehan garam NaCl (yang dikenal dengan istilah
sel Downs) :
Katoda (-) : 2 Na
+(l) + 2 e
– ——> 2 Na
(s) ……………….. (1)
Anoda (+) : 2 Cl
–(l) Cl
2(g) + 2 e
– ……………….. (2)
Reaksi sel : 2 Na
+(l) + 2 Cl
–(l) ——> 2 Na
(s) + Cl
2(g) ……………….. [(1) + (2)]


Reaksi
elektrolisis lelehan garam NaCl menghasilkan endapan logam natrium di katoda dan gelembung gas Cl
2 di anoda. Bagaimana halnya jika
lelehan garam NaCl diganti dengan
larutan garam NaCl? Apakah proses yang terjadi masih sama? Untuk mempelajari reaksi
elektrolisis larutan garam NaCl, kita mengingat kembali
Deret Volta (
lihat Elektrokimia I : Penyetaraan Reaksi Redoks dan Sel Volta).
Pada
katoda, terjadi persaingan antara air dengan ion Na
+. Berdasarkan
Tabel Potensial Standar Reduksi, air memiliki
E°red yang lebih besar dibandingkan ion Na
+. Ini berarti, air lebih mudah
tereduksi dibandingkan ion Na
+. Oleh sebab itu, spesi yang bereaksi di
katodaadalah air. Sementara, berdasarkan
Tabel Potensial Standar Reduksi, nilai
E°red ion Cl
– dan air hampir sama. Oleh karena oksidasi air memerlukan potensial tambahan (
overvoltage), maka
oksidasi ion Cl– lebih mudah dibandingkan oksidasi air. Oleh sebab itu, spesi yang bereaksi di
anoda adalah ion Cl
–. Dengan demikian, reaksi yang terjadi pada
elektrolisis larutan garam NaCl adalah sebagai berikut :
Katoda (-) : 2 H
2O
(l) + 2 e
– ——> H
2(g) + 2 OH
–(aq) ………… (1)
Anoda (+) : 2 Cl
–(aq) ——> Cl
2(g) + 2 e
– ……………….. (2)
Reaksi sel : 2 H
2O
(l) + 2 Cl
–(aq) ——> H
2(g) + Cl
2(g) + 2 OH
–(aq) ……………………. [(1) + (2)]

Reaksi
elektrolisis larutan garam NaCl menghasilkan gelembung gas H
2 dan ion OH
‑ (basa) di katoda serta gelembung gas Cl
2 di anoda. Terbentuknya ion OH
– pada
katoda dapat dibuktikan dengan perubahan warna larutan dari bening
menjadi merah muda setelah diberi sejumlah indikator fenolftalein (pp).
Dengan demikian, terlihat bahwa produk elektrolisis lelehan umumnya
berbeda dengan produk elektrolisis larutan.

Selanjutnya kita mencoba mempelajari elektrolisis larutan Na
2SO
4. Pada
katoda, terjadi persaingan antara air dan ion Na
+. Berdasarakan nilai
E°red, maka air yang akan
tereduksi di
katoda. Di lain sisi, terjadi persaingan antara ion SO
42- dengan air di
anoda. Oleh karena bilangan oksidasi
S pada
SO4-2 telah mencapai keadaan maksimumnya, yaitu +6, maka spesi SO
42- tidak dapat mengalami oksidasi. Akibatnya, spesi air yang akan
teroksidasi di
anoda. Reaksi yang terjadi adalah sebagai berikut :
Katoda (-) : 4 H
2O
(l) + 4 e
– ——> 2 H
2(g) + 4 OH
–(aq) ……….. (1)
Anoda (+) : 2 H
2O
(l) ——> O
2(g) + 4 H
+(aq) + 4 e
– ……………….. (2)
Reaksi sel : 6 H2O(l) ——> 2 H2(g) + O2(g) + 4 H+(aq) + 4 OH–(aq) …………………….. [(1) + (2)]
6 H2O(l) ——> 2 H2(g) + O2(g) + 4 H2O(l) …………………. [(1) + (2)]
2 H
2O
(l) ——> 2 H
2(g) + O
2(g) …………………….. [(1) + (2)]

Dengan demikian, baik ion Na
+ maupun SO
42-,
tidak bereaksi. Yang terjadi justru adalah peristiwa elektrolisis air
menjadi unsur-unsur pembentuknya. Hal yang serupa juga ditemukan pada
proses elektrolisis larutan Mg(NO
3)
2 dan K
2SO
4.
Bagaimana halnya jika elektrolisis lelehan maupun larutan menggunakan
elektroda yang tidak inert, seperti Ni, Fe, dan Zn? Ternyata, elektroda
yang tidak inert hanya dapat bereaksi di
anoda, sehingga produk yang dihasilkan di
anoda adalah ion elektroda yang larut (
sebab logam yang tidak inert mudah teroksidasi). Sementara, jenis elektroda tidak mempengaruhi produk yang dihasilkan di
katoda. Sebagai contoh, berikut adalah proses elektrolisis larutan garam NaCl dengan menggunakan elektroda Cu :
Katoda (-) : 2 H
2O
(l) + 2 e
– ——> H
2(g) + 2 OH
–(aq) …………………….. (1)
Anoda (+) : Cu
(s) ——> Cu
2+(aq) + 2 e
– …………………….. (2)
Reaksi sel : Cu
(s) + 2 H
2O
(l) ——> Cu
2+(aq) + H
2(g) + 2 OH
–(aq) …………………….. [(1) + (2)]
Dari pembahasan di atas, kita dapat menarik beberapa kesimpulan yang berkaitan dengan reaksi elektrolisis :
- Baik elektrolisis lelehan maupun larutan, elektroda inert tidak akan
bereaksi; elektroda tidak inert hanya dapat bereaksi di anoda
- Pada elektrolisis lelehan, kation pasti bereaksi di katoda dan anion pasti bereaksi di anoda
- Pada elektrolisis larutan, bila larutan mengandung ion alkali,
alkali tanah, ion aluminium, maupun ion mangan (II), maka air yang
mengalami reduksi di katoda
- Pada elektrolisis larutan, bila larutan mengandung ion sulfat,
nitrat, dan ion sisa asam oksi, maka air yang mengalami oksidasi di
anoda

Salah satu aplikasi sel elektrolisis adalah pada proses yang disebut
penyepuhan. Dalam proses
penyepuhan,
logam yang lebih mahal dilapiskan (diendapkan sebagai lapisan tipis)
pada permukaan logam yang lebih murah dengan cara elektrolisis. Baterai
umumnya digunakan sebagai sumber listrik selama proses
penyepuhanberlangsung. Logam yang ingin disepuh berfungsi sebagai
katoda dan lempeng perak (logam pelapis) yang merupakan logam penyepuh berfungsi sebagai
anoda.
Larutan elektrolit yang digunakan harus mengandung spesi ion logam yang
sama dengan logam penyepuh (dalam hal ini, ion perak). Pada proses
elektrolisis, lempeng perak di anoda akan teroksidasi dan larut menjadi
ion perak. Ion perak tersebut kemudian akan diendapkan sebagai lapisan
tipis pada permukaan katoda. Metode ini relatif mudah dan tanpa biaya
yang mahal, sehingga banyak digunakan pada industri perabot rumah tangga
dan peralatan dapur.

Setelah kita mempelajari aspek kualitatif reaksi elektrolisis, kini
kita akan melanjutkan dengan aspek kuantitatif sel elektrolisis. Seperti
yang telah disebutkan di awal, tujuan utama elektrolisis adalah untuk
mengendapkan logam dan mengumpulkan gas dari larutan yang
dielektrolisis. Kita dapat menentukan kuantitas produk yang terbentuk
melalui konsep mol dan stoikiometri.
Satuan yang sering ditemukan dalam aspek kuantitatif sel elektrolisis
adalah Faraday (F). Faraday didefinisikan sebagai muatan (dalam
Coulomb) mol elektron. Satu Faraday equivalen dengan satu mol elektron.
Demikian halnya, setengah Faraday equivalen dengan setengah mol
elektron. Sebagaimana yang telah kita ketahui, setiap satu mol partikel
mengandung 6,02 x 10
23partikel. Sementara setiap elektron mengemban muatan sebesar 1,6 x 10
-19 C. Dengan demikian :
1 Faraday = 1 mol elektron = 6,02 x 10
23 partikel elektron x 1,6 x 10
-19 C/partikel elektron
1 Faraday = 96320 C (sering dibulatkan menjadi 96500 C untuk mempermudah perhitungan)
Hubungan antara Faraday dan Coulomb dapat dinyatakan dalam persamaan berikut :
Faraday = Coulomb / 96500
Coulomb = Faraday x 96500
Coulomb adalah satuan muatan listrik. Coulomb dapat diperoleh melalui
perkalian arus listrik (Ampere) dengan waktu (detik). Persamaan yang
menunjukkan hubungan Coulomb, Ampere, dan detik adalah sebagai berikut :
Coulomb = Ampere x Detik
Q = I x t
Dengan demikian, hubungan antara Faraday, Ampere, dan detik adalah sebagai berikut :
Faraday = (Ampere x Detik) / 96500
Faraday = (I x t) / 96500
Dengan mengetahui besarnya Faraday pada reaksi elektrolisis, maka mol
elektron yang dibutuhkan pada reaksi elektrolisis dapat ditentukan.
Selanjutnya, dengan memanfaatkan koefisien reaksi pada masing-masing
setengah reaksi di katoda dan anoda, kuantitas produk elektrolisis dapat ditemukan.
Hukum Faraday I :

Hukum Faraday II :

Berikut ini adalah beberapa contoh soal aspek kuantitatif sel elektrolisis :
1. Pada elektrolisis larutan AgNO
3 dengan elektroda inert
dihasilkan gas oksigen sebanyak 5,6 L pada STP. Berapakah jumlah listrik
dalam Coulomb yang dialirkan pada proses tersebut?
Penyelesaian :
Reaksi elektrolisis larutan AgNO
3 dengan elektroda inert adalah sebagai berikut :
Katoda (-) : Ag
+ + e
– ——> Ag
Anoda (+) : 2 H
2O
(l) ——> O
2(g) + 4 H
+(aq) + 4 e
–
Gas O
2 terbentuk di
anoda. Mol gas O
2 yang terbentuk sama dengan 5,6 L / 22,4 L = ¼ mol O
2
Berdasarkan persamaan reaksi di
anoda, untuk menghasilkan ¼ mol gas O
2, maka jumlah mol elektron yang terlibat adalah sebesar 4 x ¼ = 1 mol elektron.
1 mol elektron = 1 Faraday = 96500 C
Jadi, jumlah listrik yang terlibat adalah sebesar 96500 C
2. Unsur Fluor dapat diperoleh dengan cara elektrolisis lelehan NaF.
Berapakah waktu yang diperlukan untuk mendapatkan 15 L gas fluorin ( 1
mol gas mengandung 25 L gas) dengan arus sebesar 10 Ampere?
Penyeleasian :
Reaksi elektrolisis lelehan NaF adalah sebagai berikut :
K (-) : Na
+(l) + e
– ——> Na
(s)
A (-) : 2 F
–(l) ——> F
2(g) + 2 e
–
Gas F
2 terbentuk di
anoda. Mol gas F
2 yang terbentuk adalah sebesar 15 L / 25 L = 0,6 mol F
2
Berdasarkan persamaan reaksi di
anoda, untuk menghasilkan 0,6 mol gas F
2, akan melibatkan mol elektron sebanyak 2 x 0,6 = 1,2 mol elektron
1,2 mol elektron = 1,2 Faraday
Waktu yang diperlukan dapat dihitung melalui persamaan berikut :
Faraday = (Ampere x Detik) / 96500
1,2 = (10 x t) / 96500
t = 11850 detik = 3,22 jam
Jadi, diperlukan waktu selama 3,22 jam untuk menghasilkan 15 L gas fluorin
3. Arus sebesar 0,452 A dilewatkan pada sel elektrolisis yang mengandung lelehan CaCl
2 selama 1,5 jam. Berapakah jumlah produk yang dihasilkan pada masing-masing elektroda?
Penyelesaian :
Reaksi elektrolisis lelehan CaCl
2 adalah sebagai berikut :
K (-) : Ca
2+(l) + 2 e
– ——> Ca
(s)
A (+) : 2 Cl
–(l) ——> Cl
2(g) + 2 e
–
Mol elektron yang terlibat dalam reaksi ini dapat dihitung dengan persamaan berikut :
Faraday = (Ampere x Detik) / 96500
Faraday = (0,452 x 1,5 x 3600) / 96500 mol elektron
Berdasarkan persamaan reaksi di
katoda, mol Ca yang dihasilkan adalah setengah dari mol elektron yang terlibat. Dengan demikian, massa Ca yang dihasilkan adalah :
Massa Ca = mol Ca x Ar Ca
Massa Ca = ½ x (0,452 x 1,5 x 3600) / 96500 x 40 = 0,506 gram Ca
Berdasarkan persamaan reaksi di
anoda, mol gas Cl
2 yang dihasilkan adalah setengah dari mol elektron yang terlibat. Dengan demikian, volume gas Cl
2 (STP) yang dihasilkan adalah :
Volume gas Cl
2 = mol Cl
2 x 22,4 L
Volume gas Cl
2 = ½ x (0,452 x 1,5 x 3600) / 96500 x 22.4 L = 0,283 L gas Cl
2
Jadi, produk yang dihasilkan di katoda adalah 0,506 gram endapan Ca dan produk yang dihasilkan di anoda adalah 0,283 L gas Cl
2 (STP)
4. Dalam sebuah percobaan elektrolisis, digunakan dua sel yang
dirangkaikan secara seri. Masing-masing sel menerima arus listrik yang
sama. Sel pertama berisi larutan AgNO
3, sedangkan sel kedua berisi larutan XCl
3.
Jika setelah elektrolisis selesai, diperoleh 1,44 gram logam Ag pada
sel pertama dan 0,12 gram logam X pada sel kedua, tentukanlah massa
molar (Ar) logam X tersebut!
Penyelesaian :
Reaksi elektrolisis larutan AgNO
3 :
K (-) : Ag
+(aq) + e
– ——> Ag
(s)
A (+) : 2 H
2O
(l) ——> O
2(g) + 4 H
+(aq) + 4 e
–
Logam Ag yang dihasilkan sebanyak 1,44 gram; dengan demikian, mol logam Ag yang dihasilkan sebesar 1,44 / 108 mol Ag
Berdasarkan persamaan reaksi di
katoda, mol elektron yang dibutuhkan untuk menghasilkan logam Ag sama dengan mol logam Ag (
koefisien reaksinya sama)
Sehingga, mol elektron yang digunakan dalam proses elektrolisis ini adalah sebesar 1,44 / 108 mol elektron
Reaksi elektrolisis larutan XCl
3 :
K (-) : X
3+(aq) + 3 e
– ——> X
(s)
A (+) : 2 Cl
–(l) ——> Cl
2(g) + 2 e
–
Arus yang sama dialirkan pada sel kedua, sehingga, mol elektron yang
digunakan dalam proses elektrolisis ini sama seperti sebelumya, yaitu
sebesar 1,44 / 108 mol elektron
Berdasarkan persamaan reaksi di
katoda, mol logam X yang dihasilkan sama dengan 1 / 3 kali mol elektron, yaitu sebesar 1 / 3 x 1,44 / 108 mol X
Massa logam X = 0,12 gram; dengan demikian, massa molar (Ar) logam X adalah sebagai berikut:
mol = massa / Ar
Ar = massa / mol
Ar = 0,12 / (1 / 3 x 1,44 / 108) = 27
Jadi, Ar dari logam X adalah 27
posted by Arvan Rusdiansyah














































